【喜訊】漢聯(lián)藥業(yè)全國多中心“干細(xì)胞治療脊髓損傷”臨床研究(IND項(xiàng)目)正式啟動(dòng)!
2023年12月21日,“注射用間充質(zhì)干細(xì)胞(臍帶)治療外傷性脊髓損傷單臂、開放、多中心探索性臨床研究”啟動(dòng)會(huì)在中山大學(xué)附屬第三醫(yī)院(以下簡稱“中山三院”)召開。

該項(xiàng)目是全國首個(gè)干細(xì)胞治療脊髓損傷的注冊(cè)臨床試驗(yàn),其申辦方為漢聯(lián)藥業(yè)旗下的天津昂賽細(xì)胞基因工程有限公司(以下簡稱“天津昂賽”),CRO為天津凱諾醫(yī)藥科技發(fā)展有限公司(以下簡稱“凱諾醫(yī)藥”)。參會(huì)人員包括中山三院院長、骨科學(xué)科帶頭人、國家藥監(jiān)局細(xì)胞類產(chǎn)品質(zhì)量研究與評(píng)價(jià)重點(diǎn)實(shí)驗(yàn)室主任戎利民教授,骨科主任劉斌教授,脊柱外科、臨床研究中心、生物治療中心有關(guān)專家和管理人員,漢氏聯(lián)合董事長韓忠朝(線上參會(huì))、漢聯(lián)藥業(yè)總經(jīng)理韓之波、臨床醫(yī)學(xué)總監(jiān)谷俊東,凱諾醫(yī)藥CO-CEO梁青(線上參會(huì))、副總經(jīng)理李光澤、醫(yī)學(xué)副總監(jiān)馬海寧等有關(guān)領(lǐng)導(dǎo)和運(yùn)營團(tuán)隊(duì)。
戎利民教授在開場致辭中闡述了該臨床試驗(yàn)在干細(xì)胞治療脊髓損傷領(lǐng)域的重大意義,并強(qiáng)調(diào)務(wù)必保證項(xiàng)目全過程的規(guī)范性和安全性。韓忠朝院士在線上進(jìn)行致辭,感謝各位專家對(duì)項(xiàng)目的支持,預(yù)祝項(xiàng)目順利開展。會(huì)議上,研究團(tuán)隊(duì)與申辦方、CRO從研究設(shè)計(jì)、知情同意、干細(xì)胞制劑制備和檢測、藥物輸注、GCP法規(guī)、受試者隨訪等多方面對(duì)試驗(yàn)方案進(jìn)行了深入、務(wù)實(shí)的討論。
該項(xiàng)目由戎利民教授牽頭,是世界上規(guī)模最大、病程覆蓋最全的“臍帶間充質(zhì)干細(xì)胞治療脊髓損傷”的臨床研究,均通過國家衛(wèi)健委和藥監(jiān)局備案。目前已完成蛛網(wǎng)膜下腔注射臍帶間充質(zhì)干細(xì)胞(UC-MSC)治療脊髓損傷的臨床前劑量探索及安全性、有效性研究,發(fā)表相關(guān)臨床研究方案及系列研究,證實(shí)UC-MSC可有效促進(jìn)神經(jīng)功能的恢復(fù)。

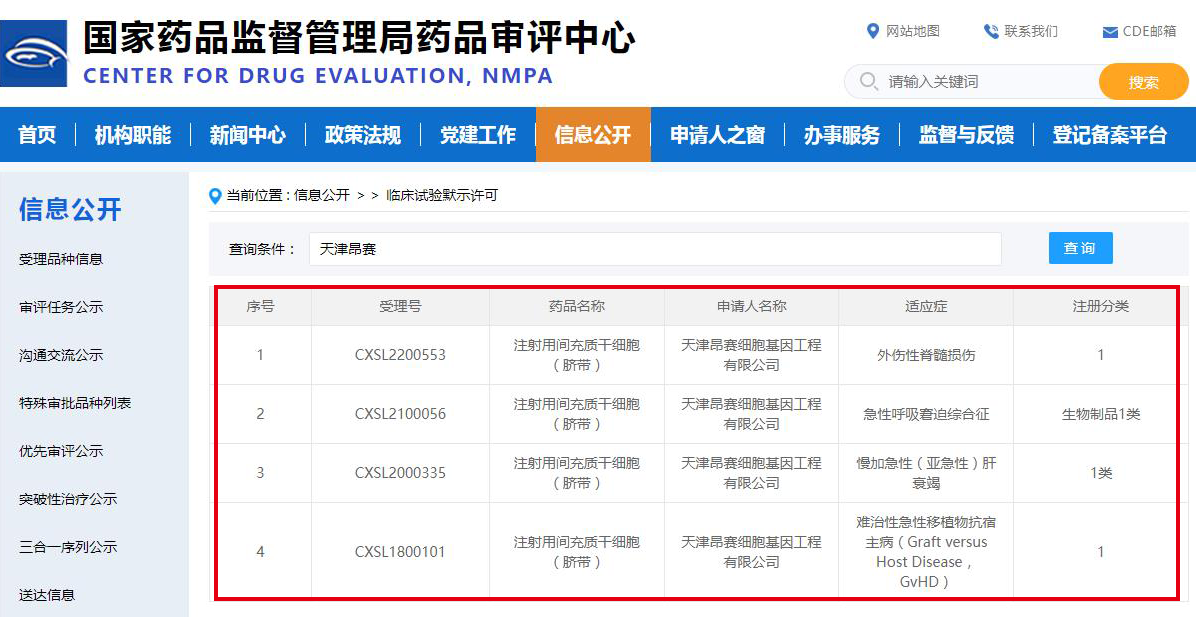
注射用間充質(zhì)干細(xì)胞(臍帶)制劑是由漢聯(lián)藥業(yè)自主研發(fā)的具有自主知識(shí)產(chǎn)權(quán)的治療用生物制品Ⅰ類新藥。注射用間充質(zhì)干細(xì)胞(臍帶)治療外傷性脊髓損傷適應(yīng)癥的IND已經(jīng)獲得國家藥品監(jiān)督管理局藥品審評(píng)中心(CDE)批準(zhǔn),同時(shí)該新藥治療難治性急性移植物抗宿主病(GvHD)、慢加急肝衰竭(ACLF)、急性呼吸窘迫綜合征(ARDS)也已獲得臨床試驗(yàn)?zāi)S并已啟動(dòng)臨床試驗(yàn)。
漢氏聯(lián)合集團(tuán)旗下的漢聯(lián)藥業(yè)板塊以細(xì)胞類新藥研發(fā)業(yè)務(wù)為主,設(shè)有多個(gè)干細(xì)胞新藥平臺(tái),位于天津、北京及法國等地區(qū),涉及研發(fā)多種劑型的細(xì)胞新藥,十幾種適應(yīng)癥,后續(xù)管線豐富。目前已自主研發(fā)了10余個(gè)干細(xì)胞新藥,其中7個(gè)細(xì)胞1類新藥已獲批進(jìn)入臨床試驗(yàn)階段,在國內(nèi)干細(xì)胞新藥研發(fā)領(lǐng)域處于領(lǐng)先地位,助推我國干細(xì)胞科技產(chǎn)業(yè)高速度以及高質(zhì)量發(fā)展。


